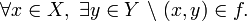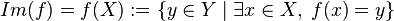Introducción:
Metanol: CH3 - OH
Etanol: CH3 - CH2 - OH
2- Propanol: OH
CH3 - CH - CH3
Metanol: alcohol metílico, alcohol de madera o carbinol.
Etanol: alcohol etílico, alcohol vínico, espíritu de vino o alcohol de granos.
2-Propanol: alcohol isopropílico
El metanol es uno de los subproductos que se obtienen por destilación de la madera en la fabricación de leña.
Cuando se somete la madera a destilación seca se obtiene:
Gases volátiles combustibles
Alcohol metílico
Ácido piroleñoso Propanona
8% Ácido acético
Líquidos volátiles
Madera Creosota
Alquitrán vegetal Hidrocarburos
20% Brea vegetal
Residuo sólido Carbón de madera
30%
Como se observa en el cuadro el alcohol metílico se halla en el ácido piroleñoso.
Para separar al metanol de la mezcla en la que se encuentra se realizan las siguientes operaciones:
Ácido piroleñoso
+
Lechada de cal [ Ca(OH)2 en solución]
Precipita etanoato de calcio
Filtración
Etanoato de calcio
(sólido)
Acetona + metanol
(líquido)
destilación fraccionada
propanona metanol
(55°) (64°)
No, no es apto para la fabricación de bebidas alcohólicas, porque es un líquido móvil, incoloro, de olor semejante al del etanol, de sabor ardiente, es un tóxico y su ingestión produce trastornos en el sistema nervioso atacando la vista, pudiendo producir ceguera total.
El alcohol que se utiliza para la fabricación base de bebidas alcohólicas es el etanol. Se lo usa en licores y bebidas como el whisky, ginebra, ron, aguardiente, coñac, etc.
Industrialmente el etanol se obtiene por fermentación alcohólica, proceso por el cual algunas sustancias orgánicas experimentan transformaciones por la acción de otras llamadas fermentos, éstos actúan como verdaderos catalizadores orgánicos activando aquellas reacciones que se producirían en menor proporción sin su presencia. Tiene un proceso final que consiste en someter a la glucosa, proveniente de un proceso previo de hidrólisis, a la acción de un fermento figurado del tipo de las levaduras denominado Saccharomyces cerevisiae. Este microorganismo segrega un fermento soluble o enzima llamado Zimasa, que actúa sobre la glucosa desdoblándola en alcohol y dióxido de carbono. Para llegar a la etapa anterior se parte de sustancias que, como la remolacha, fruto sin melazas, contienen azúcar o sustancias ricas en almidón que por hidrólisis se pueden transformar en definitiva en glucosa como las papas, granos de maíz, sorgo y otros cereales.
A continuación desarrollaremos el proceso industrial para llegar del almidón de cereales al etanol:
Almidón
Sacarificación
Amilasa: proveniente de los granos de cebada germinada: malta
Maltosa
Maltasa: proveniente de la levadura de
cerveza
Glucosa
Zimasa: proveniente de la levadura de
cerveza
Alcohol + dióxido de carbono
Metanol: la ingestión de éste produce trastornos en el sistema nervioso atacando a la vista, pudiendo producir ceguera total.
Etanol: no causan efectos negativos, salvo ante una gran ingestión provoca un estado de alcoholemia.
Metanol: se lo emplea para desnaturalizar el alcohol etílico. En este caso se lo aplica sin rectificar con el nombre de metileno, conteniendo mucha acetona.
Con el metanol se prepara metaldehído que a su vez se usa para preparar plásticos del tipo bakelita.
Etanol: se utiliza en farmacias como desinfectante y para la preparación de numerosas preparaciones (tintura de yodo, yodoformo, alcohol alcanforado, cloroformo, etc.).
En la industria se aplica para preparar barnices, explosivos, seda artificial y como extractivo de numerosas sustancias por su capacidad de disolvente en frío o en caliente.
Se lo usa como combustible y carburante.
Con él se prepara éter sulfúrico y varios ésteres.
Su principal aplicación es la preparación de bebidas alcohólicas explicadas en la pregunta n° 4.
Propanol: se emplea como antiséptico, pues sus soluciones al 50% tienen igual capacidad antiséptica que las del alcohol etílico al 60%. Se lo prefiere por razones económicas.
Por deshidrogenación catalítica se lo usa para preparar acetona.
Tiene aplicación como solvente de lacas, resinas y gomas.
Se lo usa en ciertos casos para desnaturalizar al alcohol etílico.
Soluciones:
1. Una solución es un sistema homogéneo fraccionable formado por dos o más sustancias puras miscibles, que no reaccionan entre si.
2. La concentración nos indica la relación entre la cantidad de soluto y la del solvente o la de la solución.
3.
- % masa en masa (%m/m): indica cuantos gramos de soluto están disueltos cada 100 gramos de solución.
- % masa en volumen (%M/V): indica cuantos gramos de soluto están disueltos cada 100cm3 de solución.
- Molaridad (M): como la unidad de cantidad de materia es el mol, es muy usual utilizar soluciones cuyas concentraciones están expresadas en: moles de soluto/ dm3 de solución.
- % volumen en volumen (%V/V): se define como el volumen de soluto que se encuentra disuelto en 100cm3 de solución.
- Molalidad (m): se define como el numero de moles de soluto disueltos 1kg de solvente.
- Fracción Molar (x): es la relación entre el numero de moles de un componente y el numero total de moles presentes en la solución. También se la llama fracción de sustancias.
Concentraciones que nos afectan: El alcohol en la sangre
1. a) Ingerimos 17.75 ml de alcohol.
b) Ingerimos 50 ml de alcohol.
c) Ingerimos 24 ml de alcohol.
d) Ingerimos 40 ml de alcohol.
Es lo mismo, la cantidad de moléculas de alcohol que estamos ingiriendo son las mismas por mas que lo diluya con agua.
3. En medio litro de whisky hay 200 ml de alcohol, mientras que en 1 litro de vino hay 120 ml de alcohol.
4. 300 ml de whisky y 2400 ml de cerveza tienen la misma cantidad de alcohol que 1 litro de vino.
5.
Grapa: 40° a 50°.
Tequila: 36° a 56°.
Cognac: 40°.
Oporto: 15° a 20°.
Bitter: 39° aproximadamente.
Aperitivo (Gancia): 14.8°.
Champagne: 11° a 15°.
Calor producido por el alcohol:
a) 100 cm3 de cerveza 5 cm3 de alcohol
355 cm3 de cerveza X= 17,75 cm3 de alcohol
17,75 cm3 de alcohol x 0,79g/cm3 =14, 0225 gramos
1 gramo 7 calorías
14,0225 gramos
X= 98,1575 calorías.
b) 100 cm3 de champagne 12 cm3 de alcohol
200 cm3 de champagne X= 24 cm3 de alcohol
24 cm3 de alcohol x 0,79g/cm3 =18,96 gramos
1 gramo 7 calorías
18,96 gramos
X= 132,72 calorías.
c) 100 cm3 de tequila 43 cm3 de alcohol
150 cm3 de tequila X= 64,5 cm3 de alcohol
64,5 cm3 de alcohol x 0,79g/cm3 =50,955 gramos
1 gramo 7 calorías
50, 955 gramos
X= 356,685 calorías
Como actúa el alcohol en nuestro organismo:
Un persona de 70 kilogramos metaboliza en dos horas 14 gramos de alcohol.
1. El fundamento químico de este aparato analizador es una reacción de óxido-reducción. Al hacer soplar al conductor por la boquilla del aparato se introduce en este aire que puede contener vapores de alcohol. En el analizador hay una solución ácida de dicromato de potasio. El Etanol es oxidado a ácido acético y el cromo, anaranjado amarillento en el ion dicromato, es reducido a ion crómico, de color verde. Mediante un analizador clorimétrico, calibrado adecuadamente, se puede inferir la concentración de etanol en sangre y de este modo es posible detectar cuando un conductor esta alcoholizado.
a) en nuestro país se permite un máximo de 0.5 gramos de alcohol por cada litro de sangre. Y 0.0 gramos de alcohol por cada litro de sangre para los conductores profesionales.
b)
EEUU: 0.15 gramos
c)
Suecia: 0.2 gramos.
d)
España: 0.5 gramos.
e)
Alemania: 0.18 gramos.
f)
Italia: 0.5 gramos.
3.
| Peso de la persona (kg) | Cantidad |
| | Vino (vasos/copas) | Cervezas |
| 65 a 85 | 6 | 3 |
| 100 | 8 | 4 |
 con un (y sólo un)
con un (y sólo un)  se denota
se denota  , en lugar de
, en lugar de 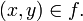
 o
o  . A los elementos del dominio se les llama habitualmente argumento de la función.
. A los elementos del dominio se les llama habitualmente argumento de la función.o codomf
 o
o  o
o 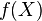 .
. es algún
es algún  tal que
tal que  .
. , tiene como dominio, codominio e imagen a todos los números reales
, tiene como dominio, codominio e imagen a todos los números reales 
 tal que
tal que  , en cambio, si bien su dominio y codominio son iguales a
, en cambio, si bien su dominio y codominio son iguales a  , sólo tendrá como imagen los valores comprendidos entre 0 y +∞.
, sólo tendrá como imagen los valores comprendidos entre 0 y +∞.  , con
, con